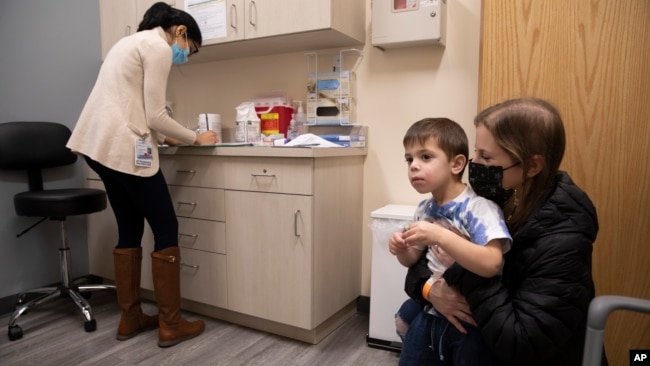
モデルナ社、6才以下へのワクチン承認を当局に求めている
mRNAワクチンは、数分から数日といった時間の経過とともに分解されて、人の遺伝情報(DNA)に組みこまれるものではないと言われていますが。
仮に私に5才の子がいるとして、接種を希望するでしょうか?
今日も、VOAで英語を学びましょう!!
モデルナ、6歳以下の小児用コロナ注射認可を求めて(和訳)
Moderna Seeks COVID Shots for Children under 6
April 28, 2022
アメリカの製薬会社モデルナは、同社のワクチンCOVID-19を全米の幼児向けに承認するよう、アメリカ当局に求めています。5歳以下の子どもたちは、米国でまだワクチンを接種できない唯一のグループです。
家族は、人々がより多く集まり、顔を覆うものが少なくなっているにもかかわらず、幼い子供たちを守るために長い間待っていました。しかし、コロナウイルスの変異種は広がり続けています。
モデルナは、その研究結果を食品医薬品局(FDA)に提供しました。製薬会社は、2回の低用量注射で乳幼児を守ることができることを証明する情報であることを期待しています。
「これらの最も幼い子供たちには、重要なunmet medical need(いまだに治療法が見つかっていない疾患に対する医療ニーズ)があります。」とポール・バートン医師は言います。子供への2回の注射は、”安全に子供たちを守ることができるでしょう。時間が経てば追加投与が必要になる可能性が高いと思います。”
現在、ファイザーのワクチンが唯一子供用に承認されています。しかし、そのワクチンは5歳以上の子供だけが対象です。そのため、1800万人の幼児や赤ちゃんが無防備な状態になっています。
ファイザー社は、さらに少量の3種類の注射が非常に幼い子供に効くかどうかも発表する予定です。FDAは2月に、同社の2種類の注射は十分な強度がないと発表しています。
家族の中には、なぜ幼い子供のための注射にこれほど時間がかかるのかと疑問を持つ人もいます。
FDAのワクチン担当責任者であるピーター・マークス博士は今週、米国の議員に対して、生産者が申請を完了するまでFDAは製品を評価することができないと述べました。木曜日の声明で、FDAは、モデルナはまだその要求を完了するためにいくつかの追加データを送信する必要がありると言います。
「適切な評価をすることが極めて重要であり、それによって親は我々が認可する全てのワクチンを信頼することができるのです。」とマークス氏は言います。
もしFDAがモデルナのワクチンを幼児と乳児に承認すれば、米国疾病対策センター(CDC)は、誰がこのワクチンを必要とするかを推奨しなければなりません。すべての幼児を対象とするか、COVID-19のリスクが高い子供だけを対象とするか、どちらかになるでしょう。
FDAは、いくつかの複雑な問題に直面することになります。
幼児向けの2回のモデナ注射は、それぞれ大人の通常量の4分の1です。生後6ヶ月から5歳までの子供たちを対象にした研究では、この投与量でウイルスと闘う抗体が高レベルで生成されることがデータで示されています。これは、若年成人の場合と同じ量であったとバートンは述べています。重篤な副作用の報告もなく、他の通常の小児用ワクチンに比べて高体温になることも少なかったと言います。
モデルナのワクチンは、試験中、症状のあるCOVID-19の予防に約40パーセントから50パーセントの効果があることが証明されました。バートン氏は、オミクロン 変異種が部分的にワクチン免疫から逃れる能力があることが、効果が高くならない理由であると述べています。
モデルナ社のCOVIDワクチンは、今のところ米国では成人しか接種できません。他の国では、すでに6歳の子供にも接種できるようになっていますが、数ヶ月前にFDAは、10代の少年にまれな心臓関連の副作用があることを懸念していると発表しています。
COVID-19は一般に、子供にとっては大人ほど危険ではありません。しかし、少数の人が重病になったり、死んだりしています。CDCによれば、パンデミックの開始以来、5歳未満の約475人の子供がCOVID-19で死亡しています。オミクロンが蔓延している間、子供の入院は大きく増加しました。
どれだけの親が幼い子供や赤ちゃんにワクチンを接種する予定なのかは不明です。5歳から11歳の子供のうち、2回の予防接種を受けているのは3分の1以下です。
Moderna Seeks COVID Shots for Children under 6
American drugmaker Moderna is asking U.S. officials to approve its COVID-19 vaccine for the nation's youngest children. Children under 5 are the only group in the United States not yet able to be vaccinated.
Families have been waiting a long time to protect their young children, even as people are gathering in higher numbers and wearing fewer face coverings. But coronavirus variants continue to spread.
Moderna provided its study results to the Food and Drug Administration (FDA). The drug company hopes the information proves that two low-dose shots can protect babies and young children.
“There is an important unmet medical need here with these youngest kids,” said Dr. Paul Burton. He is Moderna's chief medical officer. Two shots for children “will safely protect them. I think it is likely that over time they will need additional doses.”
Currently, Pfizer’s vaccine is the only one approved for children. But that vaccine is only for children over the age of 5. That leaves 18 million young children and babies unprotected.
Pfizer is also expected to announce whether three of its even smaller-dose shots work for very young children. The FDA said in February that the company’s two doses were not strong enough.
Some families have questioned why a shot for young children has taken so long.
FDA vaccine chief Dr. Peter Marks told U.S. lawmakers this week that the FDA cannot evaluate a product until a producer completes its application. In a statement Thursday, the FDA said Moderna still must send some additional data to complete its request.
“It’s critically important that we have the proper evaluation so that parents will have trust in any vaccines that we authorize,” Marks said.
If the FDA approves Moderna’s vaccine for young children and babies, the U.S. Centers for Disease Control and Prevention (CDC) would then have to recommend who needs it. It could either be for all young children or just those at higher risk from COVID-19.
The FDA will face some complex questions.
The two Moderna shots for young children are each one-fourth of the normal dose for an adult. In a study of kids ages 6 months through 5 years, data showed that the doses produced high levels of virus-fighting antibodies. It was the same amount produced in young adults, Burton said. There were no serious side effects reported, and the shots resulted in fewer high body temperatures than other usual vaccines for children.
Moderna’s vaccine proved between about 40 percent and 50 percent effective at preventing symptomatic COVID-19 during the trial. Burton said the Omicron variant's ability to partly escape vaccine immunity was a reason that effectiveness was not higher.
Moderna's COVID vaccine so far has only been available to adults in the U.S. Other countries have already been offering the shot to children as young as 6. But months ago the FDA said it had concerns about a rare heart-related side effect in teenage boys.
COVID-19 generally is not as dangerous for children as it is for adults. But a small number have become very sick or even died. About 475 children younger than 5 have died from COVID-19 since the pandemic’s start, the CDC says. Child hospitalizations greatly increased during the spread of Omicron.
It is not clear how many parents plan to vaccinate their young children and babies. Less than one-third of children ages 5 to 11 have had two vaccinations.
Words in This Story
variant — n. something that is different in some way from others of the same kind
dose — n. the amount of a medicine, drug, or vitamin that is taken at one time
evaluate — v. to judge the value or condition of in a careful and thoughtful way
application — n. a formal and usually written request for something
proper — adj. correct according to social or moral rules
authorize — v. to give power or permission to
teenage — n. between 13 and 19 years old